Gas ideal adalah konsep penting dalam ilmu fisika dan termodinamika yang digunakan untuk menggambarkan perilaku gas dalam kondisi tertentu. Meskipun gas ideal tidak ada dalam kenyataan, model ini memberikan pemahaman yang berguna tentang bagaimana gas berperilaku di bawah berbagai kondisi. Artikel ini akan membahas secara mendetail tentang gas ideal, termasuk pengertian, hukum-hukum yang mengatur perilakunya, serta aplikasi dan keterbatasan dari model gas ideal, disertai dengan penjelasan ilustratif untuk setiap konsep.
Pengertian Gas Ideal
Gas ideal adalah gas yang mengikuti hukum gas ideal, yang menyatakan bahwa tekanan (P), volume (V), dan suhu (T) gas berhubungan satu sama lain dengan cara yang dapat dijelaskan oleh persamaan:
![]()
Di mana:
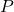 = tekanan gas (dalam pascal)
= tekanan gas (dalam pascal)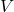 = volume gas (dalam meter kubik)
= volume gas (dalam meter kubik)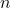 = jumlah mol gas
= jumlah mol gas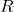 = konstanta gas ideal (8.314 J/(mol·K))
= konstanta gas ideal (8.314 J/(mol·K))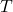 = suhu gas (dalam Kelvin)
= suhu gas (dalam Kelvin)
Gas ideal dianggap sebagai gas yang partikel-partikelnya tidak saling berinteraksi dan memiliki volume yang sangat kecil dibandingkan dengan volume gas itu sendiri.
- Ilustrasi: Bayangkan gas ideal sebagai “bola-bola kecil” yang bergerak bebas di dalam ruangan. Seperti bola yang tidak saling bertabrakan dan memiliki ruang yang cukup untuk bergerak, partikel gas ideal bergerak tanpa hambatan.
Hukum-Hukum Gas Ideal
Beberapa hukum dasar yang mengatur perilaku gas ideal meliputi:
1. Hukum Boyle
Hukum Boyle menyatakan bahwa pada suhu konstan, tekanan gas berbanding terbalik dengan volume gas. Jika volume gas meningkat, tekanan gas akan menurun, dan sebaliknya. Hukum ini dapat dinyatakan dengan rumus:
![]()
- Ilustrasi: Bayangkan sebuah balon. Ketika Anda menekan balon (mengurangi volume), tekanan di dalam balon meningkat. Seperti balon yang mengembang saat udara ditambahkan, hukum Boyle menunjukkan hubungan antara tekanan dan volume.
2. Hukum Charles
Hukum Charles menyatakan bahwa pada tekanan konstan, volume gas berbanding lurus dengan suhu gas dalam Kelvin. Jika suhu gas meningkat, volume gas juga akan meningkat. Hukum ini dapat dinyatakan dengan rumus:
![]()
- Ilustrasi: Bayangkan gas dalam balon yang dipanaskan. Ketika balon dipanaskan, gas di dalamnya mengembang, menyebabkan balon mengembang. Seperti balon yang mengembang saat suhu meningkat, hukum Charles menunjukkan hubungan antara volume dan suhu.
3. Hukum Gay-Lussac
Hukum Gay-Lussac menyatakan bahwa pada volume konstan, tekanan gas berbanding lurus dengan suhu gas dalam Kelvin. Jika suhu gas meningkat, tekanan gas juga akan meningkat. Hukum ini dapat dinyatakan dengan rumus:
![]()
- Ilustrasi: Bayangkan kaleng yang berisi gas yang dipanaskan. Ketika kaleng dipanaskan, tekanan di dalam kaleng meningkat. Seperti kaleng yang bisa meledak jika dipanaskan terlalu lama, hukum Gay-Lussac menunjukkan hubungan antara tekanan dan suhu.
Aplikasi Gas Ideal
Model gas ideal memiliki berbagai aplikasi dalam ilmu fisika dan teknik, antara lain:
1. Perhitungan Termodinamika
Gas ideal digunakan dalam perhitungan termodinamika untuk memahami proses-proses yang melibatkan gas, seperti pemanasan, pendinginan, dan ekspansi. Model ini membantu insinyur dan ilmuwan merancang sistem yang efisien.
- Ilustrasi: Bayangkan insinyur yang merancang mesin. Seperti insinyur yang menggunakan rumus untuk menghitung efisiensi mesin, model gas ideal membantu dalam perhitungan yang diperlukan untuk merancang sistem yang efisien.
2. Proses Industri
Dalam industri, gas ideal digunakan untuk memahami dan mengontrol proses yang melibatkan gas, seperti reaksi kimia dan pemisahan gas. Model ini membantu dalam merancang reaktor dan sistem pemisahan yang efisien.
- Ilustrasi: Bayangkan pabrik yang memproduksi gas. Seperti pabrik yang mengontrol proses untuk menghasilkan produk yang berkualitas, model gas ideal membantu dalam merancang proses industri yang efisien.
3. Meteorologi
Model gas ideal juga digunakan dalam meteorologi untuk memahami perilaku atmosfer. Gas ideal membantu dalam memprediksi cuaca dan memahami fenomena atmosfer lainnya.
- Ilustrasi: Bayangkan ilmuwan yang mempelajari cuaca. Seperti ilmuwan yang menggunakan model untuk memprediksi cuaca, model gas ideal membantu dalam memahami perilaku gas di atmosfer.
Keterbatasan Model Gas Ideal
Meskipun model gas ideal sangat berguna, ada beberapa keterbatasan yang perlu diperhatikan:
1. Interaksi Antara Partikel
Model gas ideal mengasumsikan bahwa partikel gas tidak saling berinteraksi. Namun, dalam kenyataannya, partikel gas dapat saling berinteraksi, terutama pada tekanan tinggi dan suhu rendah.
- Ilustrasi: Bayangkan sekelompok orang yang bergerak bebas di ruangan. Seperti orang-orang yang saling bertabrakan saat bergerak, partikel gas dapat saling berinteraksi dalam kondisi tertentu.
2. Volume Partikel
Model gas ideal mengasumsikan bahwa volume partikel gas sangat kecil dibandingkan dengan volume gas itu sendiri. Namun, pada tekanan tinggi, volume partikel dapat mempengaruhi perilaku gas.
- Ilustrasi: Bayangkan sekelompok bola yang diisi dalam ruangan. Seperti bola yang memerlukan ruang untuk bergerak, volume partikel gas dapat mempengaruhi perilaku gas dalam kondisi tertentu.
3. Suhu dan Tekanan Ekstrem
Model gas ideal tidak berlaku pada suhu dan tekanan ekstrem, di mana gas dapat berperilaku secara berbeda. Dalam kondisi ini, model gas nyata, seperti model van der Waals, lebih tepat digunakan.
- Ilustrasi: Bayangkan gas yang berada di dalam ruang angkasa. Seperti gas yang berperilaku berbeda di luar angkasa, gas dapat berperilaku berbeda pada suhu dan tekanan ekstrem.
Kesimpulan
Gas ideal adalah konsep penting dalam termodinamika yang membantu kita memahami perilaku gas di bawah berbagai kondisi. Dengan memahami pengertian, hukum-hukum yang mengatur perilakunya, serta aplikasi dan keterbatasan model gas ideal, kita dapat lebih menghargai peran gas dalam berbagai proses fisika dan teknik. Seperti bola-bola kecil yang bergerak bebas, gas ideal memberikan gambaran tentang bagaimana gas berperilaku dalam kondisi ideal. Pengetahuan tentang gas ideal juga penting dalam pengembangan teknologi dan aplikasi yang melibatkan gas, serta dalam memahami fenomena alam yang terjadi di sekitar kita.

