Distilasi adalah teknik pemisahan yang mendasar dan penting dalam berbagai industri. Proses distilasi sederhana melibatkan pemanasan campuran cair hingga titik didih, kemudian mengumpulkan uap yang terbentuk dan mengembalikannya menjadi cairan dengan pendinginan. Komponen dengan titik didih lebih rendah akan menguap terlebih dahulu dan terpisah dari komponen dengan titik didih lebih tinggi.

Distilasi adalah proses pemisahan komponen cair berdasarkan perbedaan titik didihnya. Proses ini umum digunakan dalam industri kimia dan farmasi untuk memurnikan bahan kimia, menghasilkan minuman beralkohol, dan memproduksi minyak atsiri. Distilasi memanfaatkan sifat-sifat fisik komponen cair yang berbeda untuk memisahkan mereka secara efisien.
Distilasi menggunakan penguapan dan kondensasi untuk memisahkan campuran.
Apa itu distilasi?
Distilasi merupakan salah satu metode pemisahan fasa yang merupakan salah satu metode pemisahan campuran. Distilasi terdiri dari penggunaan dua proses fisik secara berurutan dan terkontrol: penguapan dan kondensasi, menggunakannya secara selektif untuk memisahkan komponen-komponen campuran yang umumnya homogen, yaitu komponen-komponennya tidak dapat dibedakan dengan mata telanjang.
Campuran yang dapat dipisahkan menjadi komponen-komponennya masing-masing menggunakan distilasi mungkin mengandung dua cairan, satu padatan dalam cair, atau bahkan gas cair. Metode pemisahan ini didasarkan pada perbedaan titik didih (sifat bawaan materi, yaitu suhu di mana tekanan uap suatu cairan sama dengan tekanan di sekitar cairan) dari berbagai zat. Zat yang titik didihnya paling rendah terlebih dahulu akan masuk ke fasa uap, kemudian zat tersebut akan mengembun di wadah lain, dan relatif tetap murni.
Dengan cara ini agar penyulingan dapat dilakukan dengan benar maka campuran tersebut harus direbus sampai titik didih salah satu zat penyusunnya tercapai, yang kemudian akan menjadi uap dan dapat dibawa ke wadah yang didinginkan, di mana ia akan disimpan. Itu mengembun dan menjadi cair kembali.
Sebaliknya, zat komponen lainnya akan tetap berada di dalam wadah tanpa perubahan; tetapi dalam kedua kasus tersebut kita akan mendapatkan zat murni, bebas dari campuran awal.
Ini dapat membantu Anda: Filtrasi
Pengertian
Distilasi adalah salah satu metode pemisahan dan pemurnian yang paling penting dalam kimia dan industri. Proses ini memanfaatkan perbedaan titik didih dari komponen-komponen dalam campuran untuk memisahkan atau memurnikan bahan. Artikel ini akan menjelaskan prinsip dasar distilasi, jenis-jenis distilasi, aplikasi, serta contoh penggunaannya dalam kehidupan sehari-hari dan industri.
Prinsip Dasar Distilasi
Distilasi bekerja berdasarkan prinsip bahwa komponen-komponen dalam suatu campuran memiliki titik didih yang berbeda. Ketika campuran dipanaskan, komponen dengan titik didih lebih rendah akan menguap terlebih dahulu. Uap tersebut kemudian didinginkan dan dikondensasi menjadi cairan murni. Proses ini dapat diulang beberapa kali untuk meningkatkan kemurnian zat yang dihasilkan.
Hukum Raoult
Ketika kita mempunyai campuran cairan yang ideal (campuran yang interaksi antara partikel-partikel berbeda dianggap sama dengan interaksi antara partikel-partikel yang sama) Hukum Raoult terpenuhi.
Hukum ini menyatakan bahwa tekanan uap parsial masing-masing komponen dalam campuran gas sama dengan tekanan uap komponen murni dikalikan fraksi molnya dalam campuran cair.
Tekanan uap total kemudian merupakan jumlah dari tekanan parsial komponen campuran dalam fasa gas. Di sisi lain, fraksi mol suatu komponen dalam suatu campuran adalah ukuran konsentrasinya yang tidak berdimensi. Besaran yang disebutkan di atas dapat dihitung menggunakan persamaan berikut:
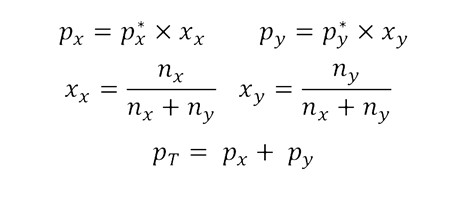
Di mana:
- p x dan p y masing-masing adalah tekanan parsial komponen x dan y dalam campuran uap yang mengelilingi campuran cairan.
- p x * dan p y * adalah tekanan uap komponen x dan y.
- x x dan x y adalah fraksi mol komponen x dan y dalam campuran cairan.
- n x dan ny adalah jumlah zat komponen x dan y dalam campuran cairan.
Hukum Raoult yang disebutkan di atas berlaku untuk campuran ideal (yang merupakan model yang dibuat manusia untuk menyederhanakan penelitian), namun kenyataannya hukum ini mengalami penyimpangan jika campuran tersebut nyata.
Jadi, jika partikel-partikel berbeda dalam campuran mempunyai gaya antarmolekul yang lebih kuat daripada partikel-partikel dalam cairan murni, maka tekanan uap campuran tersebut lebih kecil dari tekanan uap cairan murni, yang menghasilkan penyimpangan negatif dari Hukum Raoult.
Sebaliknya, jika gaya antarmolekul antara partikel-partikel dalam cairan murni lebih besar daripada gaya antarmolekul dalam campuran, maka partikel-partikel dalam campuran akan lebih mudah keluar ke fase uap, sehingga tekanan uapnya akan meningkat. pencampuran akan semakin besar, menghasilkan deviasi positif dari hukum Raoult
Ketika ingin menyuling campuran azeotropik (misalnya etanol dan air), perlu ditambahkan beberapa komponen (benzena, dalam hal ini) agar azeotropnya termodifikasi dan dengan cara ini komponen-komponen campuran tersebut dapat dipisahkan. Azeotrop adalah campuran cairan dengan komposisi tertentu yang bila mendidih, uap yang dihasilkan mempunyai komposisi campuran yang sama (sehingga komponen-komponen campuran azeotropik tidak dapat dipisahkan dengan distilasi sederhana atau fraksional).
Azeotrop mempunyai titik didih tertentu, misalnya pada tekanan 1 atm, etanol mendidih pada 78,37 °C dan air mendidih pada 100 °C, sedangkan azeotrop etanol-air mendidih pada 78,2 °c. Campuran azeotropik mempunyai penyimpangan negatif atau positif dari Hukum Raoult, tergantung kasusnya.
Jenis distilasi
Distilasi dapat terjadi dengan berbagai cara:
- Distilasi sederhana. Cara paling mendasar adalah merebus campuran hingga komponen-komponen yang berbeda terpisah. Ini adalah metode pemisahan yang efektif ketika titik didih komponen-komponen campuran sangat berbeda (idealnya, perbedaan titik didih komponen-komponen tersebut minimal 25°C, jika tidak maka tidak menjamin kemurnian total zat yang disuling).
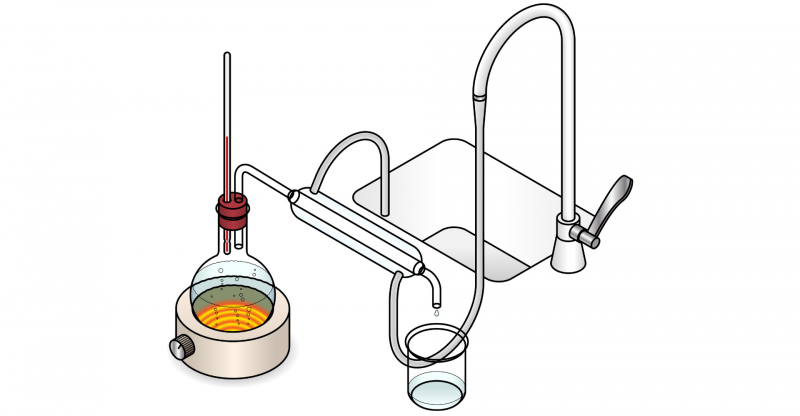
- Distilasi fraksional. Hal ini dilakukan dengan menggunakan kolom fraksinasi, yang terdiri dari pelat berbeda di mana penguapan dan kondensasi terjadi secara berurutan, menjamin kemurnian yang lebih besar pada komponen yang dipisahkan.
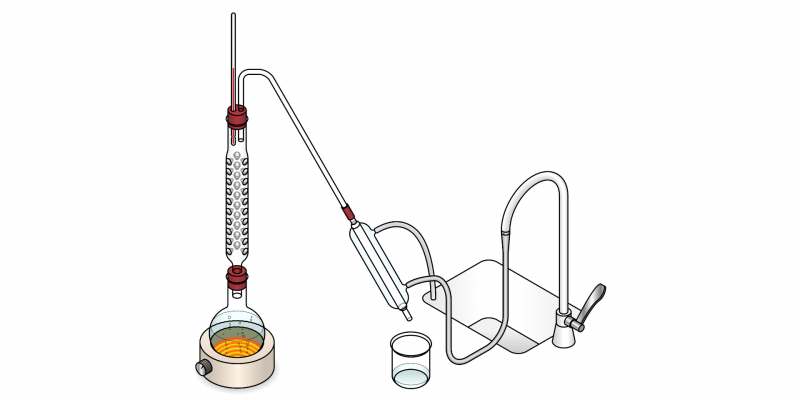
- Distilasi vakum. Dengan mengurangi tekanan hingga tercipta ruang hampa, proses ini dikatalisis untuk mengurangi titik didih komponen, karena beberapa komponen memiliki titik didih yang sangat tinggi yang dapat dikurangi ketika tekanan diturunkan secara signifikan dan, dengan cara ini, mempercepat proses. distilasi.
- Distilasi azeotropik. Distilasi diperlukan untuk memecah azeotrop, yaitu campuran yang zat-zatnya berperilaku satu, meskipun memiliki titik didih yang sama, sehingga tidak dapat dipisahkan dengan distilasi sederhana atau fraksional. Untuk memisahkan campuran azeotropik perlu dilakukan modifikasi kondisi campuran, misalnya dengan menambahkan komponen pemisah.
- Distilasi uap. Komponen campuran yang mudah menguap dan tidak mudah menguap dipisahkan dengan injeksi langsung uap air.
- Distilasi kering. Ini terdiri dari memanaskan bahan padat tanpa adanya pelarut cair, memperoleh gas dan kemudian mengembunkannya dalam wadah lain.
- Distilasi yang ditingkatkan. Disebut juga distilasi alternatif atau reaktif, ini disesuaikan dengan kasus spesifik campuran yang sulit dipisahkan atau memiliki titik didih yang sama.
Contoh distilasi

Batubara menggunakan distilasi kering untuk mendapatkan bahan bakar organik cair.
- Penyulingan minyak. Pemisahan berbagai hidrokarbon yang ada dalam minyak dilakukan melalui distilasi fraksional, menyimpan setiap senyawa yang berasal dari pemasakan minyak mentah dalam berbagai lapisan atau kompartemen terpisah pada kolom distilasi. Gas-gas ini naik dan mengembun di lapisan atas kolom, sedangkan zat yang lebih padat seperti aspal dan parafin tetap berada di lapisan bawah.
- Retakan katalitik. Ini adalah nama yang diberikan untuk penyulingan vakum tertentu yang umum dalam pengolahan minyak, menggunakan menara vakum untuk memisahkan gas memasak dari minyak mentah. Ini mempercepat pendidihan hidrokarbon dan mempercepat prosesnya. Cracking adalah jenis distilasi destruktif, di mana hidrokarbon yang lebih besar dipecah (pada suhu tinggi dan menggunakan katalis) menjadi hidrokarbon yang lebih kecil, yang memiliki titik didih lebih rendah.
- Pemurnian etanol. Untuk memisahkan alkohol seperti etanol dari air selama produksinya di laboratorium, digunakan distilasi azeotropik, menambahkan benzena atau komponen lain ke dalam campuran yang mendorong atau mempercepat pemisahan, dan yang kemudian dapat dengan mudah dihilangkan tanpa mengubah komposisi kimia produk..
- Pengolahan batubara. Untuk memperoleh bahan bakar organik cair digunakan batu bara atau kayu melalui prosedur penyulingan kering, sehingga gas yang dikeluarkan pada pembakaran dapat terkondensasi.
- Termolisis garam mineral. Melalui distilasi kering, berbagai zat mineral dengan kegunaan industri tinggi diperoleh, dari emanasi dan kondensasi gas yang diperoleh dengan membakar garam mineral.
- alembik. Ini adalah nama yang diberikan untuk perangkat yang ditemukan pada zaman Arab, yang tujuannya adalah untuk memproduksi parfum, obat-obatan, dan alkohol dari buah-buahan yang difermentasi. Dalam pengoperasiannya digunakan prinsip distilasi: zat dipanaskan dalam ketel kecil dan gas yang dihasilkan didinginkan dalam kumparan yang menuju ke wadah lain tempat cairan yang dihasilkan dari kondensasi gas tersebut dikumpulkan.
- Produksi parfum. Distilasi uap digunakan untuk memperoleh wewangian, merebus air bersama bunga yang diawetkan, hingga menghasilkan gas dengan bau yang diinginkan dan kemudian bila dikondensasi, dapat digunakan sebagai cairan dasar dalam wewangian.
Aplikasi Distilasi
- Industri Kimia:
- Distilasi digunakan untuk memurnikan bahan kimia, seperti asam, alkohol, dan pelarut.
- Penting dalam produksi bahan kimia organik dan anorganik.
- Industri Minyak dan Gas:
- Distilasi fraksional digunakan di kilang minyak untuk memisahkan komponen-komponen minyak mentah menjadi produk yang berguna seperti bensin, diesel, dan minyak tanah.
- Produksi Minuman Beralkohol:
- Distilasi digunakan untuk memproduksi minuman beralkohol seperti wiski, vodka, dan rum.
- Memurnikan etanol dari fermentasi.
- Pengolahan Air:
- Distilasi sederhana digunakan dalam proses desalinasi untuk memurnikan air laut menjadi air tawar.
- Industri Makanan dan Minuman:
- Distilasi uap digunakan untuk mengekstraksi minyak esensial dan perasa dari bahan alami.
Contoh Penggunaan Distilasi
- Desalinasi Air Laut:
- Proses distilasi sederhana menguapkan air laut untuk memisahkan garam dan mendapatkan air tawar.
- Penyulingan Minyak Atsiri:
- Distilasi uap digunakan untuk mengekstraksi minyak atsiri dari daun, bunga, dan batang tanaman.
- Produksi Minyak Mentah:
- Distilasi fraksional di kilang minyak memisahkan minyak mentah menjadi berbagai produk seperti bensin, diesel, dan minyak pelumas.
