Asam adalah salah satu konsep fundamental dalam ilmu kimia yang memiliki berbagai sifat dan aplikasi. Dalam kehidupan sehari-hari, asam dapat ditemukan dalam berbagai bentuk, mulai dari makanan dan minuman hingga produk pembersih dan obat-obatan. Artikel ini akan membahas secara mendetail tentang pengertian asam, sifat-sifatnya, jenis-jenis asam, serta peranannya dalam kehidupan, disertai dengan penjelasan ilustratif untuk setiap konsep.
1. Definisi Asam
a. Pengertian Asam
Asam adalah senyawa kimia yang dapat melepaskan ion hidrogen (H?) ketika dilarutkan dalam air. Menurut teori Brønsted-Lowry, asam didefinisikan sebagai donor proton, sedangkan menurut teori Arrhenius, asam adalah senyawa yang meningkatkan konsentrasi ion hidrogen dalam larutan. Asam memiliki pH kurang dari 7, yang menunjukkan sifat asamnya.
Ilustrasi: Bayangkan asam sebagai “donor hadiah”. Seperti seseorang yang memberikan hadiah kepada orang lain, asam memberikan proton (H?) kepada larutan di sekitarnya.
b. Sejarah Penemuan Asam
Konsep asam telah ada sejak zaman kuno, tetapi pemahaman ilmiah tentang asam berkembang seiring dengan kemajuan ilmu pengetahuan. Pada abad ke-18, ilmuwan seperti Antoine Lavoisier dan Svante Arrhenius memberikan kontribusi penting dalam memahami sifat dan perilaku asam. Penemuan ini membuka jalan bagi pengembangan teori asam-basa yang lebih kompleks.
Ilustrasi: Bayangkan sejarah penemuan asam sebagai “perjalanan pengetahuan”. Seperti perjalanan yang membawa penemunya ke pemahaman baru, penemuan tentang asam membuka wawasan baru tentang sifat-sifat kimia.
2. Sifat-sifat Asam
a. Sifat Fisik
1. Rasa: Asam umumnya memiliki rasa asam atau masam. Contohnya, asam sitrat dalam lemon memberikan rasa asam yang khas.
2. Bau: Beberapa asam memiliki bau yang tajam dan menyengat, seperti asam asetat yang memberikan aroma cuka.
3. Warna: Asam dapat mempengaruhi warna indikator pH. Misalnya, indikator lakmus merah akan berubah menjadi biru dalam larutan basa, tetapi tetap merah dalam larutan asam.
Ilustrasi: Bayangkan sifat fisik asam sebagai “karakteristik rasa”. Seperti rasa yang membedakan makanan, sifat fisik asam memberikan ciri khas yang membedakannya dari senyawa lain.
b. Sifat Kimia
1. Reaksi dengan Basa: Asam bereaksi dengan basa untuk membentuk garam dan air dalam reaksi netralisasi. Contohnya, asam klorida (HCl) bereaksi dengan natrium hidroksida (NaOH) untuk membentuk natrium klorida (NaCl) dan air.
Reaksi Kimia:
![]()
2. Reaksi dengan Logam: Asam dapat bereaksi dengan logam untuk menghasilkan gas hidrogen. Misalnya, asam sulfat (H2SO4) bereaksi dengan seng (Zn) untuk menghasilkan seng sulfat dan gas hidrogen.
Reaksi Kimia:
![]()
3. Penguraian Senyawa: Asam dapat menguraikan senyawa organik dan anorganik, yang sering digunakan dalam proses pembersihan dan pengolahan.
Ilustrasi: Bayangkan sifat kimia asam sebagai “reaksi yang dinamis”. Seperti reaksi yang mengubah satu bahan menjadi bahan lain, sifat kimia asam menunjukkan kemampuannya untuk berinteraksi dengan berbagai senyawa.
3. Jenis-jenis Asam
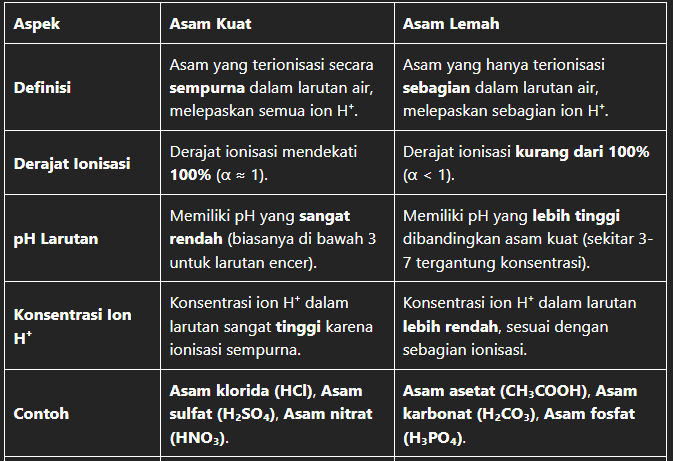
a. Asam Kuat dan Asam Lemah
1. Asam Kuat: Asam yang sepenuhnya terionisasi dalam larutan, menghasilkan konsentrasi ion hidrogen yang tinggi. Contoh asam kuat termasuk asam klorida (HCl), asam sulfat (H2SO4), dan asam nitrat (HNO3).
Ilustrasi: Bayangkan asam kuat sebagai “pemain utama”. Seperti pemain yang mendominasi permainan, asam kuat memiliki kemampuan untuk menghasilkan ion hidrogen dalam jumlah besar.
2. Asam Lemah: Asam yang hanya sebagian terionisasi dalam larutan, menghasilkan konsentrasi ion hidrogen yang lebih rendah. Contoh asam lemah termasuk asam asetat (CH3COOH) dan asam sitrat (C6H8O7).
Ilustrasi: Bayangkan asam lemah sebagai “pemain pendukung”. Seperti pemain yang berkontribusi tetapi tidak mendominasi, asam lemah memiliki pengaruh yang lebih kecil dalam menghasilkan ion hidrogen.
b. Asam Organik dan Anorganik
1. Asam Organik: Asam yang mengandung karbon dan biasanya ditemukan dalam senyawa alami. Contoh asam organik termasuk asam asetat, asam sitrat, dan asam laktat.
Ilustrasi: Bayangkan asam organik sebagai “senyawa alami”. Seperti bahan alami yang ditemukan di alam, asam organik sering kali berasal dari sumber alami seperti buah-buahan dan produk fermentasi.
2. Asam Anorganik: Asam yang tidak mengandung karbon dan biasanya lebih kuat. Contoh asam anorganik termasuk asam klorida, asam sulfat, dan asam nitrat.
Ilustrasi: Bayangkan asam anorganik sebagai “senyawa sintetis”. Seperti bahan kimia yang diproduksi di laboratorium, asam anorganik sering kali digunakan dalam industri dan penelitian.
4. Peranan Asam dalam Kehidupan
a. Dalam Makanan dan Minuman
Asam memainkan peran penting dalam memberikan rasa pada makanan dan minuman. Misalnya, asam sitrat memberikan rasa asam pada lemon, sedangkan asam asetat memberikan rasa pada cuka. Selain itu, asam juga berfungsi sebagai pengawet dalam makanan.
Ilustrasi: Bayangkan asam dalam makanan sebagai “bumbu rasa”. Seperti bumbu yang memberikan cita rasa pada masakan, asam memberikan rasa yang khas pada makanan dan minuman.
b. Dalam Proses Biokimia
Asam memiliki peran penting dalam berbagai proses biokimia dalam tubuh. Misalnya, asam amino adalah blok bangunan protein, dan asam nukleat (DNA dan RNA) adalah molekul yang menyimpan informasi genetik.
Ilustrasi: Bayangkan asam dalam biokimia sebagai “blok bangunan kehidupan”. Seperti batu bata yang membangun sebuah bangunan, asam membangun struktur dasar kehidupan.
c. Dalam Industri
Asam digunakan dalam berbagai aplikasi industri, termasuk produksi pupuk, pembersih, dan bahan kimia. Asam sulfat, misalnya, digunakan dalam produksi baterai dan pengolahan mineral.
Ilustrasi: Bayangkan asam dalam industri sebagai “bahan baku”. Seperti bahan baku yang diperlukan untuk memproduksi barang, asam adalah komponen penting dalam banyak proses industri.
d. Dalam Kesehatan
Asam juga memiliki peran dalam kesehatan. Beberapa asam, seperti asam folat, penting untuk pertumbuhan dan perkembangan sel. Selain itu, asam asetilsalisilat (aspirin) digunakan sebagai obat untuk mengurangi rasa sakit dan peradangan.
Ilustrasi: Bayangkan asam dalam kesehatan sebagai “obat penyembuh”. Seperti obat yang membantu menyembuhkan penyakit, asam memiliki peran penting dalam menjaga kesehatan.
5. Kesimpulan
Asam adalah senyawa kimia yang memiliki berbagai sifat, jenis, dan peranan penting dalam kehidupan sehari-hari. Dari memberikan rasa pada makanan hingga berperan dalam proses biokimia dan industri, asam memiliki dampak yang signifikan dalam banyak aspek kehidupan. Dengan memahami pengertian, sifat, jenis, dan peranan asam, kita dapat lebih menghargai peranannya dalam kehidupan kita. Dalam dunia yang semakin kompleks, pemahaman tentang asam dan cara kerjanya menjadi semakin penting. Dengan pengetahuan yang tepat, kita dapat memanfaatkan asam dengan cara yang lebih bijaksana dan sehat, serta menjaga keseimbangan yang diperlukan untuk kesehatan dan kesejahteraan kita.